人工知能の国際会議AAAI-26から、医療や化学の現場で使われることを想定した複数の研究を解説するセッションを紹介する。これはカンファレンス初日、2026年1月22日の午前中に行われた以下の5つの発表をまとめた60分のセッションである。AAAIではそれぞれの研究発表は10分間のプレゼンテーションと2分間の質疑応答というフォーマットで統一されており、Application for AIの他にはComputer Vision、Machine Learning、Graph-based Machine Learning、Multimodal Learning、Reinforces Learning、Natural Language Processing、Motion &Tracking、Ethics, Bias and Fiarnessといったカテゴリーに分けてプレゼンテーションが実施されていた。特に動画やイメージ生成に関連するカテゴリーと機械学習に関連するカテゴリーが発表数としては圧倒的に多い。
他にはAIに関する倫理的な側面を掘り下げたセッションや機械学習の中で特定の情報を消す、Machine Unlearningなども複数の発表で見られたことからも単に精度の良い新技術を研究するだけではなく、どう使えば社会に役に立つのか? という視点が存在していることにも注目したい。
それぞれの発表は解決する問題の定義、それを見つけた背景、新しい技術の解説、従来の技術との違いを実験で検証、数値で評価、結論としてこの研究で見つけられた知見を解説するというフォーマットとなっており、それはポスターセッションとして貼り出されるポスターの構成と同じである。
このセッションでは、以下の発表を写真と共に紹介する。
「Treatment Stitching with Schrödinger Bridge for Enhancing Offline Reinforcement Learning in Adaptive Treatment Strategies」、発表者は韓国大学の研究者だ。このセッションでは糖尿病を例に挙げて治療を症状に応じて段階的に行う適応的治療戦略(ATS)にオフライン強化学習による新しいアプローチを使うという内容となっている。

要約は、強化学習では試行錯誤によるオンライン学習を行うが、臨床の現場では患者に対して試行錯誤を行うことができない。そのために過去のデータだけで学習を行うオフライン強化学習を用いるが、臨床データが不足するためにその性能が不足してしまう。
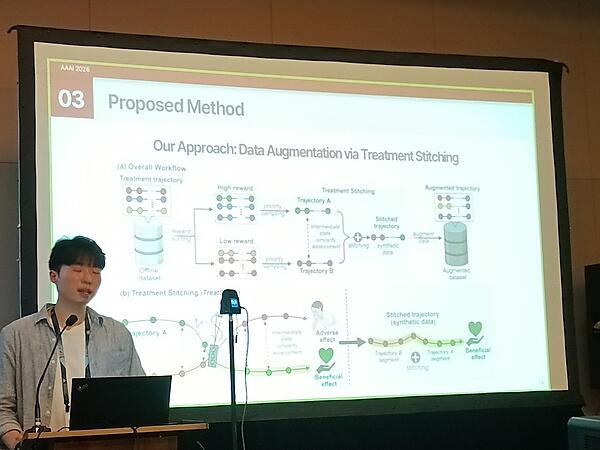
この問題を解決するためにTreatStitchという臨床データを拡張する手法を提案している。TreatStitchは既存の臨床データから「似た中間状態」を見つけて治療の軌跡(Trajectory)をつなぎ合わせて新しい治療の経路を生成するというアプローチだ。似た中間状態を見つける際に「シュレーディンガーブリッジ」という手法を使って滑らかで最短の「つなぎ経路」を生成するというのがこの研究の中核である。
これは不足する臨床データから合成データを作成することで強化学習に必要なデータを作り出す発想だ。合成データを追加することでオフライン強化学習はより多様なデータから学習可能となり適応的治療戦略(ATS)の最適化性能が向上する、というものである。
この発表で使ったシュレーディンガーブリッジを紹介。ここではイメージを変化させる発想を臨床データをつなぎ合わせる部分に使っている。

シュレーディンガーブリッジについては拡散モデル(Diffusion Model)との比較を解説。ここでは花のイメージデータが変化させていく際のインターポレーションに注目して、拡散モデルでは中間状態はノイズになるが、シュレーディンガーブリッジでは最も近似したイメージに徐々に変化していく様子を説明。これが臨床データの合成に必要なつなぎ合わせのために有効であるということだろう。

次のプレゼンテーションは「Distributional Priors Guided Diffusion for Generating 3D Molecules in Low Data Regimes」、発表者は香港理工大學の研究者だ。
研究の要約は、データが豊富な領域で学習した分子生成モデルをデータが乏しい領域(構造が異なる分子など)にも一般化させられるかという課題に対するアプローチだ。従来の分布外(Out-of Distribution)生成に関する研究では主に「性質の違い」に注目していたが、ここでは分子骨格や官能基といった「構造の違い」に焦点を当てている。
拡散モデルを使ったGODD(Geometric OOD Diffusion Model)を提案し、データが豊富な分布で学習しつつデータが少ない構造的に異なる分布にも一般化できる拡散モデルの枠組みを構築したと説明。分布外構造変化(新しい骨格・環構造など)を含むベンチマークで、提案されたモデルでは分子の妥当性・独自性・新規性に基づく成功率を12.6%向上させたという。

次のプレゼンテーションは「TRACE: Transformation-Aware Graph Refinement for Reaction Condition Prediction」というタイトルで、これも発表者は湖南大学、澳門理工大學などの研究者だ。
要約は以下の通り。
化学合成では収率や選択性に大きく影響するため適切な反応条件の特定が重要である。しかし既存手法の多くは、反応物と生成物の構造変化(トランスフォーメーション)を明示的に扱えず、反応機構の理解や条件予測に限界があった。本研究では「TRACE」という反応条件予測のための「構造変化を考慮したグラフ精緻化フレームワーク」を提案する。
TRACEの特徴は以下の通り:- 反応物と生成物の情報を統合し、原子レベルで反応特有の構造変化を表すグラフを構築
- 構造情報を強化するエンコーダで化学的文脈を付与
- 変化に関係する結合を動的に選択する「インタラクション精緻化モジュール」
- 反応中心の情報を利用するメカニズム正則化により、条件予測に重要な相互作用を強調
ベンチマーク実験では「TRACEは複数の反応条件タイプで最先端性能を達成し、構造変化を考慮した精緻化が予測精度・汎化性能・実用的な合成計画での頑健性を向上させることが示された」
これも、化学の領域でグラフ理論を応用した分子反応を予測するためのフレームワークだ。

次のプレゼンテーションはイスラエル工科大学の研究者によるもので「PDE-Driven Spatiotemporal Generative Modeling for Multilead ECG Synthesis」というタイトルになっている。複雑な心電図のアウトプットの理解を促進するための新しい手法を提案している。
「12誘導心電図(ECG)の生成は、心臓電気活動の複雑な時空間構造を再現する必要があるため難しい。従来の生成モデルは、各誘導間の精密な依存関係を十分に捉えられないことが多い。
本研究では「PhysioPDE-GAN」を提案する。これは、
- 心臓の電気生理を表す、偏微分方程式(PDE)に基づく生理学的知識
- 誘導間の空間的制約
「PhysioPDE-GAN」が生成したECGで学習した分類器は、従来手法の合成データで学習した分類器よりも、心疾患の検出性能が統計的に有意に向上した。この結果は、PDEベースの心臓モデルと生成モデルを組み合わせることで、より高品質で医療的に有用な合成バイオメディカルデータを作れる可能性を示している」

最後のプレゼンテーションは、西北師範大學の研究者による「Topology-Enhanced and Label Correlation-Aware Model for Protein-Protein Interaction Prediction」、タンパク質の相互作用を予測するモデルに関する研究だ。
要約は以下の通り。
「タンパク質同士の相互作用(PPI)の予測は、細胞機能や疾患理解に重要だが、既存の深層学習モデルには2つの課題がある。- 相互作用ネットワーク内の直接的な相互作用だけに依存しており、機能的に似たタンパク質同士の潜在的な関連を捉えられない
→ GNNの平滑化(類似ノードを似た表現にする能力)が十分に働かない - 相互作用タイプ(エッジラベル)間の潜在的な依存関係を適切にモデル化できていない
→ 予測性能が制限される
- PPIネットワークの構造とラベル分布を利用して、機能的に類似したタンパク質を結ぶ「類似エッジ」を追加
- ラベルの共起統計を用いて、ラベル埋め込みに相関情報を組み込む
複数のデータセット・分割設定での実験により「SELC-PPI」は既存手法を大きく上回る性能を示し、モデル設計の有効性が確認された」
「SELC-PPI」は機能的に似ているタンパク質の作用をラベルとして埋め込むことで「構造強化(similarity edges)」と「ラベル相関学習(label correlation embeddings)」を追加する拡張フレームワークである。結果として「複数のデータセット」「複数のデータ分割設定(ランダム分割、時間分割など)」の全てにおいて既存手法を大幅に上回る性能を示したという。特に改善が大きいのは「類似タンパク質の表現学習」「複雑な相互作用タイプの予測」「データが疎な領域での汎化性能」である。
この5つのプレゼンテーションに共通する補助的な情報として、人工知能や機械学習の分野でシステムの一部を除去し、その影響を分析する研究手法(Ablation Study)が公開されている点にも注目したい。特定のコンポーネントを除去し、システムのパフォーマンスを評価することでそのコンポーネントがシステム全体に与える貢献を明らかにできる。研究者が性能評価や従来手法との比較を定量的に行うことと同じ程度にAIに特化した研究では必要なアプローチということだろう。
数多く実施されたプレゼンテーションの中からごく一部だけを紹介したが、10分という時間の中で密度の濃い解説と参加者からの質問が活発に行われることに感銘を受けた内容となった。参加者からの質問がない場合でも、この時間の司会者役である研究者が必ず質問を行うという姿勢により緊張感を保った質の高い発表が可能になるということだろう。また、どの国からの研究者であも全て英語によるスライドと解説、質疑応答も全て英語という国際会議としての体裁が素晴らしいと感じたセッションとなった。



































